Die Ära der Immunonkologie: bessere Chancen für Krebspatienten
Die therapeutische Beeinflussung von Immun-Checkpoint-Signalwegen bietet die Chance, Langzeitüberleben und Lebensqualität von Krebspatienten deutlich zu verbessern. Der Schlüssel dazu liegt in ihrem besonderen Wirkmechanismus: der Stärkung der antitumoralen Immunantwort.1,2
Veröffentlicht:Therapie mit Checkpoint-Inhibitoren: Die Waffen des Immunsystems nutzen
Mittlerweile sind immunonkologische Medikamente bei vielen Indikationen im Einsatz. Seit der ersten Zulassung eines Antikörpers gegen CTLA-4 im Jahr 2011 und eines PD-1-Inhibitors im Jahr 2015 werden Immun-Checkpoint-Inhibitoren mittlerweile für die Behandlung einer Vielzahl an Tumorentitäten in verschiedenen Indikationen eingesetzt, wie etwa beim malignen Melanom, nicht-kleinzelligen Lungenkarzinom (NSCLC), Nierenzellkarzinom, Urothelkarzinom, Plattenepithelkarzinom des Kopf-Hals-Bereichs, klassischen Hodgkin-Lymphom und beim Plattenepithelkarzinom des Ösophagus.
Seit 2018 stehen PD-1-Inhibitoren auch zur Behandlung des malignen Melanoms im adjuvanten Setting zur Verfügung.
Die spezifischen Nebenwirkungen bei Immun-Checkpoint-Inhibition unterscheiden sich maßgeblich von den Nebenwirkungen anderer onkologischer Therapien. Eine gute Kenntnis möglicher immunvermittelter Nebenwirkungen ist für die erfolgreiche Behandlung der Patienten essenziell.3
Immunonkologische Kombinationstherapie
Eine weitere Perspektive bietet die Erweiterung der antitumoralen Immunantwort durch die kombinierte Therapie eines Antikörpers gegen CTLA-4 mit einem PD-1-Inhibitor, da sie unterschiedliche Checkpoint-Signalwege adressieren.2
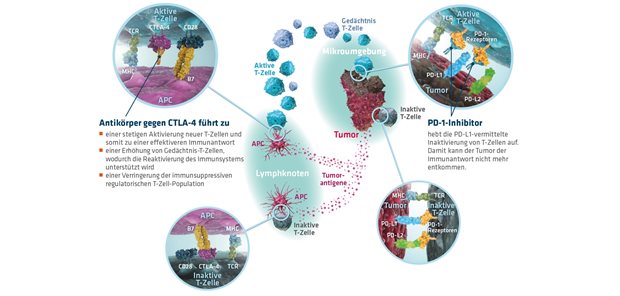
Synergistische Effekte der immunonkologischen Kombination von PD-1-Inhibitoren und Antikörper gegen CTLA-4. APC: Antigen-präsentierende Zelle; CTLA-4: cytotoxic T lymphocyte-associated protein 4; MHC: major histocompatibility complex; PD-1: programmed cell death protein 1; PD-L1: programmed death ligand 1; TCR: T-Zell-Rezeptor; mod nach Wolchok4, Peggs5, Blank6, Hamanishi7, Nurieva8
© Bristol Myers Squibb
Nobelpreis geadelter Wirkmechanismus
Immunonkologische Therapien unterscheiden sich maßgeblich von anderen onkologischen Therapien: Sie richten sich nicht direkt gegen den Tumor, sondern verstärken die T-Zell-basierte Immunantwort durch Hemmung inhibierender Immun-Checkpoints.1,2 Damit hängt die Wirksamkeit der Substanzen nicht von der Anwesenheit bestimmter Treibermutationen ab und ist nicht auf histologische Tumorsubtypen beschränkt.9 Derzeit gibt es mit CTLA-4 und PD-1 zwei Checkpoint-Signalwege als Angriffspunkte immunonkologischer Therapien. Die grundlegenden Arbeiten zur Immunonkologie durch James P. Allison, USA, und Tasuku Honjo, Japan, wurden 2018 mit dem Nobelpreis für Physiologie oder Medizin ausgezeichnet.10
bms-onkologie.de: Ihr Fachportal für Onkologie und Hämatologie
Inzwischen liegen umfangreiche Erfahrungen und Daten zur Wirksamkeit und Sicherheit von Checkpoint-Inhibitoren aus der Praxis vor. Im Onkologie-Fachportal von Bristol Myers Squibb können Sie sich weiter über Grundlagen der Immunonkologie informieren. Zudem finden Sie eine Reihe spannender Videos und Vorträge zum Einsatz von Immun-Checkpoint-Inhibitoren bei verschiedenen Tumorentitäten.
Auf dem Portal finden Sie auch alle Materialien einschließlich des behördlich genehmigten Schulungsmaterials, mit denen Bristol Myers Squibb Sie und Ihre Patienten beim Umgang mit immunvermittelten Nebenwirkungen unterstützt.
Referenzen:
1. Dizon DS, Krilov L, Cohen E et al. Clinical Cancer Advances 2016: Annual Report on Progress Against Cancer From the American Society of Clinical Oncology. J Clin Oncol 2016;34:987-1011. doi: 10.1200/JCO.2015.65.8427.
2. Pardoll DM. The blockade of immune checkpoints in cancer immunotherapy. Nat Rev Cancer 2012;12:252-264. doi: 10.1038/nrc3239.
3. Heinzerling L et al. Checkpoint Inhibitors. Dtsch Ärztebl Int 2019;116:119-126. doi: 10.3238/arztebl.2019.0119.
4. Wolchock J et al. J Clin Oncol 2013; 31: 15_suppl (Abstract).
5. Peggs KS, Quezada SA, Korman AJ, Allison JP. Principles and use of anti-CTLA4 antibody in human cancer immunotherapy. Curr Opin Immunol 2006;18:206-13. doi: 10.1016/j.coi.2006.01.011.
6. Blank C, Mackensen A. Contribution of the PD-L1/PD-1 pathway to T-cell exhaustion: an update on implications for chronic infections and tumor evasion. Cancer Immunol Immunother 2007;56:739-745. doi: 10.1007/s00262-006-0272-1.
7. Hamanishi J, Mandai M, Iwasaki M et al. Programmed cell death 1 ligand 1 and tumor-infiltrating CD8+ T lymphocytes are prognostic factors of human ovarian cancer. Proc Natl Acad Sci USA 2007;104:3360-3365. doi: 10.1073/pnas.0611533104.
8. Nurieva RI, Liu X, Dong C. Yin-Yang of costimulation: crucial controls of immune tolerance and function. Immunol Rev 2009; 229: 88-100. doi: 10.1111/j.1600-065X.2009.00769.x.
9. https://www.nobelprize.org/prizes/medicine/2018/press-release/; abgerufen am 13.01.2021.
10. Gettinger S, Herbst RS. B7-H1/PD-1 blockade therapy in non-small cell lung cancer: current status and future direction. Cancer J 2014; 20: 281-289. doi: 10.1097/PPO.0000000000000063.
Impressum
Bristol-Myers Squibb GmbH & Co. KGaA
Geschäftsführer
Neil Archer
Arnulfstr. 29
80636 München
Tel.: (089) 1 21 42-0
Registergericht München HRB 154472
Umsatzsteueridentifikations-Nr.: DE 129308813
Aufsichtsbehörde:
Regierung von Oberbayern
Maximilianstraße 39
80538 München