Neue Wege gegen problematische Keime
Es bleibt ein ewiger Wettlauf: Neue Antibiotika führen früher oder später zu Keimen mit neuen Resistenzen. Dagegen wiederum helfen nur neue Antibiotika. Einige dringend benötigte Innovationen sind in den vergangenen Jahren auf den Markt gekommen, andere stehen bereits in den Startlöchern.
Veröffentlicht: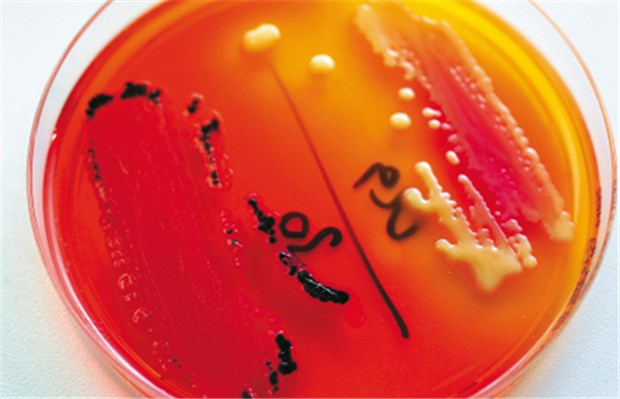
Mit solchen Bakterienkulturen lässt sich die Wirksamkeit von Antibiotika prüfen, und es können Resistenzen erfasst werden.
© Klaro
Je häufiger Ärzte neue Antibiotika anwenden, um so schneller entstehen auch Resistenzen, und um so stärker breiten sie sich aus. Doch auch bei einem sehr umsichtigen Gebrauch finden Bakterien irgendwann einen Weg, neue Wirkstoffe außer Gefecht zu setzen.
Daher ist es gut, in der Auseinandersetzung zwischen Mensch und Keim noch ein paar spitze Pfeile im Köcher zu haben - also Antibiotika, die auch dann noch wirken, wenn menschliches Leben auf dem Spiel steht und die bisherigen Waffen stumpf sind.
Diese Gefahr, dass bewährte Antibiotika nicht mehr wirken, besteht auch in Deutschland: So verdoppelte sich der Anteil Beta-Laktam- und Cephalosporin-abbauenender E. coli in kurzer Zeit von 5,1 auf 10,3 Prozent, die Rate der Methicillin-resistenten Staphylokokken (MRSA) stieg auf inzwischen 20 Prozent, und knapp 11 Prozent der Enterococcus faecium sind nach Daten aus 2007 gegenüber Vancomycin resistent.
Diese Zahlen machen klar, dass neue Wirkstoffe dringend nötig sind, so die Infektiologen Privatdozentin Rika Draenert und Professor Johannes Bogner vom Klinikum der Universität München (Der Internist 2009, 10:1282). Mit einigen neuen eingeführten Antibiotika sowie anstehenden Innovationen könnte sich das Blatt wieder mehr zugunsten der Ärzte und ihrer Patienten wenden:
• Doripenem (Doribax®), ein Carbapenem, ist breit wirksam gegen grampositive Pathogene, Anaerobier und gramnegative Bakterien einschließlich Pseudomonas aeruginosa. Es ist zugelassen gegen intraabdominelle Infekte, komplizierte Harnwegsinfekte sowie nosokomiale Pneumonien.
Die Arznei inaktiviert wichtige Penicillin-bindende Proteine und blockiert damit die Zellwandsynthese. In Studien waren die Heilungsraten bei intraabdominellen Infektionen ähnlich gut wie mit Meropenem.
Bei nosokomialen Pneumonien mit P. aeruginosa und K. pneumoniae war Doripenem einer Therapie mit Piperacillin/Tazobactam überlegen, bei komplizierten Harnwegsinfekten war die Wirksamkeit mit der von Levofloxacin vergleichbar. Häufigste unerwünschte Wirkungen waren Kopfschmerzen, Übelkeit, Durchfall, Hautausschlag sowie Leberenzymerhöhnung.
• Ceftobiprol könnte als Breitspektrum-Cephalosporin das Therapiespektrum gegen MRSA erweitern. Zum Wirkspektrum zählen aber auch Vancomycin-resistente S. aureus, P. aeruginosa und Enterokokken. Derzeit ist Ceftobiprol in Kanada und in der Schweiz bei komplizierten Haut- und Weichteilinfektionen zugelassen.
Nach einem negativen Bescheid eines EMA-Ausschusses ist mit einer EU-Zulassung vorerst nicht zu rechnen. In Studien, unter anderem bei Patienten mit diabetischem Fuß, wurden zum Teil höhere Heilungsraten als mit Vancomycin erzielt (81 versus 47 Prozent).
• Linezolid (Zyvoxid®), ein synthetisches Oxazolindinon, hemmt die Proteinsynthese der bakteriellen Ribosomen. Es wirkt gegen grampositive Keime, auch gegen MRSA. Zugelassen ist es bei komplizierten Haut- und Weichteilinfektionen und nosokomialen Pneumonien.
In mehreren Studien war Linezolid einer Therapie mit Vancomycin bei MRSA-Infektionen tendenziell überlegen, was auf die bessere Gewebegängigkeit zurückgeführt wird. Linezolid wurde auch bei Fasziitis oder MRSA-Pneumonien erfolgreich angewandt. Als limitierend erwies sich in Studien die Knochenmarktoxizität, die sich meist als Thrombozytopenie äußerte, sowie die Serotonintoxizität - ein Problem vor allem bei einer SSRI-Therapie.
• Tigecyclin (Tygacil®), eine Tetrazyklin-Weiterentwicklung, hemmt die Proteinsynthese an den bakteriellen Ribosomen. Zugelassen ist die Arznei bei komplizierten Haut- und Weichteilinfektionen sowie komplizierten intraabdominellen Infekten.
Das Mittel wirkt gegen grampositive Erreger, einschließlich MRSA, aber auch gegen Beta-Laktam- und Cephalosporin-abbauende Keime. Die Arznei reichert sich gut in extravasalen Geweben an, vor allem in Galle, Kolon und Lunge. Die Serumkonzentration sinkt jedoch rasch nach der intravenösen Infusion, was bei einer Bakteriämie problematisch ist. Mögliche unerwünschte Wirkungen sind vor allem Übelkeit und Erbrechen.
• Daptomycin (Cubicin®) gehört zur völlig neuen Substanzklasse der zyklischen Lipopeptide. Die Peptide lagern sich in die Zellmembran ein und vereinigen sich dort zu Kaliumkanälen, die den Keim abtöten. Ziel sind ebenfalls grampositive Erreger. Zugelassen ist Daptomycin bei komplizierten Haut- und Weichteilinfektionen, rechtsseitiger infektiöser Endokarditis durch S. aureus sowie S.-aureus-Bakteriämie.
Studien zeigten, dass Daptomycin im Vergleich zur alleinigen Vancomycintherapie bei MRSA-Infektionen überlegen war. Im Vergleich zu Vancomycin-Kombitherapien war die Substanz ähnlich gut wirksam. Allerdings treten unter prolongierter Therapie vermehrt Resistenzen auf, weshalb bei langer Therapiedauer zur Vorsicht geraten wird. Mögliche Nebenwirkungen sind Kopfschmerzen, Schlafstörungen, Hautausschlag und gastrointestinale Störungen.
• In der Entwicklung befinden sich auch neue Glykopeptide. Dalbavancin hat eine lange lipophile Seitenkette, was die Wirksamkeit gegenüber grampositiven Bakterien, einschließlich MRSA, verbessert. Mit seiner langen Halbwertszeit muss Dalbavancin nur einmal wöchentlich gegeben werden.
Oritavancin ist ein Lipoglykopeptid mit großem Wirkspektrum gegen grampositive Erreger, inklusive MRSA. Die Substanz akkumuliert intrazellulär, wodurch S. aureus auch in Zellen erreicht und eine Persistenz erschwert wird.
Telavancin ist eine Weiterentwicklung von Vancomycin. Auch diese Substanz richtet sich gegen grampositive Bakterien und MRSA. In vitro zeigte sich die Substanz auch aktiv gegenüber Stämmen, die auf Linezolid oder Daptomycin nicht ansprachen.
Mit Iclaprim wird zudem ein neues Diaminopyridin klinisch geprüft. Es hemmt auch Trimethoprim-resistente Keime. Das Wirkspektrum umfasst S. aureus (auch MRSA), ß-hämolysierende Streptokokken, Pneumokokken, Enterokokken, Listerien, Legionellen und Chlamydien.
Lesen Sie dazu auch: MRSA: Saarland sagt Keimen den Kampf an