Grundlagenforschung
Wie bei Fettleber die gefährliche Steatohepatitis entstehen kann
Eine nichtalkoholische Fettlebererkrankung (NAFLD) kann in eine potenziell lebensbedrohliche Steatohepatitis (NASH) übergehen. Mechanismen dazu hat ein Team des Deutschen Zentrums für Diabetesforschung (DZD) aufgeklärt. Dies könnte die Suche nach Therapieansätzen beschleunigen.
Veröffentlicht: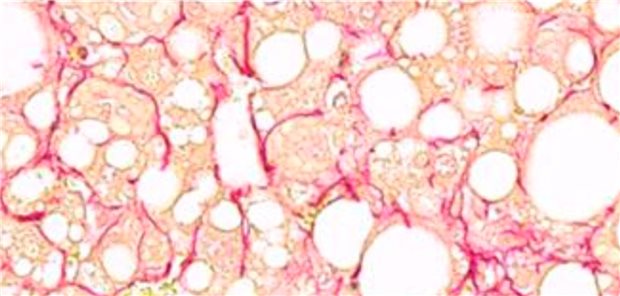
Histologischer Schnitt von Lebergewebe mit Fibrose und rot markierten Kollagenfasern.
© Anne Loft / Helmholtz Zentrum München
München. Die nichtalkoholische Fettlebererkrankung (NAFLD) ist die häufigste Lebererkrankung weltweit. Über 90 Prozent der Übergewichtigen, 60 Prozent der Menschen mit Diabetes und bis zu 20 Prozent der Normalgewichtigen entwickeln die Krankheit. Hauptmerkmal ist die Ansammlung von Fett in der Leber.
Allerdings: Eine Leber kann verfetten und dennoch normal funktionieren. Jedoch können die Fettansammlungen auch eine nichtalkoholische Steatohepatitis (NASH) verursachen – eine aggressivere Form der NAFLD. Die NASH geht mit Entzündungen und mitunter Fibrose einher und kann wiederum zu weiteren Komplikationen wie Leberzirrhose und primärem Leberkrebs führen und lebensbedrohlich sein.
Schlüssel für neue Therapieansätze
Erkranken Menschen mit NAFLD zusätzlich an einer Leberfibrose, so ist das ein Zeichen für ein langfristig erhöhtes Sterberisiko. Die Mechanismen, die den vergleichsweise guten Zustand einer NAFLD hin zur fortgeschrittenen NASH mit Fibrose verschlechtern, sind noch nicht vollständig bekannt, sagt Professor Stephan Herzig vom Helmholtz Zentrum München.
„Wenn wir verstehen, welche Mechanismen eine Fettleber zur lebensbedrohlichen Erkrankung machen, dann haben wir auch den Schlüssel gefunden, um nach besseren Therapiemöglichkeiten und präventiven Maßnahmen zu suchen“, wird der Direktor des dort ansässigen Helmholtz Diabetes Centers in einer Mitteilung des Zentrums zitiert.
Mit Genomanalysen hat ein Team die Mechanismen untersucht, die die Entwicklung und Funktion der Hepatozyten steuern (Cell Metabol. 2021; online 7. Juli). „Unsere Ergebnisse zeigen, dass Hepatozyten während der Weiterentwicklung zur NASH einen teilweisen Identitätsverlust erleiden, sie werden umprogrammiert“, erklärt Dr. Anne Loft, Erstautorin der Studie, in der Mitteilung.
Die Umprogrammierung der Hepatozyten wird durch ein Netzwerk von Proteinen, die als molekulare Schalter fungieren („Transkriptionsfaktoren“) streng kontrolliert. Die Aktivität der Proteine führt zur Dysfunktion der Hepatozyten. Das Proteinnetzwerk spielt auch eine wesentliche Rolle bei der Entwicklung einer Fibrose.
„Diese Erkenntnisse sind wichtig, weil sie die zellulären Mechanismen entschlüsseln, die der nichtalkoholischen Steatohepatitis zugrunde liegen. Das Wissen um die Rolle der Proteinnetzwerke und den Identitätsverlust der Hepatozyten liefert uns potenzielle Zielstrukturen und Interventionsmöglichkeiten für die Entwicklung wirksamer Therapien“, sagt die Doktorandin Ana Alfaro, ebenfalls Erstautorin der Studie, in der Mitteilung.
Proteinnetzwerk im Fokus
Basierend auf diesen Erkenntnissen können die Forschenden nun neue Ansätze entwickeln, um bestimmte Knotenpunkte im Proteinnetzwerk gezielt anzugreifen und so das Fortschreiten der Krankheit zu verhindern oder sogar – was bisher noch nicht möglich ist – eine bestehende Fibrose rückgängig zu machen.
Die Studie wurde vom Helmholtz Zentrum München in Zusammenarbeit mit dem Uniklinikum Heidelberg und dem Deutschen Zentrum für Diabetesforschung geleitet. Alle diese Institutionen gehören zum Deutschen Zentrum für Diabetesforschung (DZD). (eb/eis)










![Kommen die Kröpfe zurück nach Deutschland? Porträts: [M] Feldkamp; Luster | Hirn: grandeduc / stock.adobe.com](/Bilder/Portraets-M-Feldkamp-Luster-Hirn-grandeduc-stockadobecom-230510.jpg)