PEI-Präsident im Interview
Jetzt ist der Zeitpunkt für Arzneitests gegen Ebola!
Noch gibt es kein Medikament gegen Ebola. Warum das so ist und weshalb vielversprechende experimentelle Therapien keine Wundermittel sind, erklärt der Präsident des Paul-Ehrlich-Instituts im Exklusiv-Interview. Er fordert, schnell klinische Studien zu starten.
Veröffentlicht: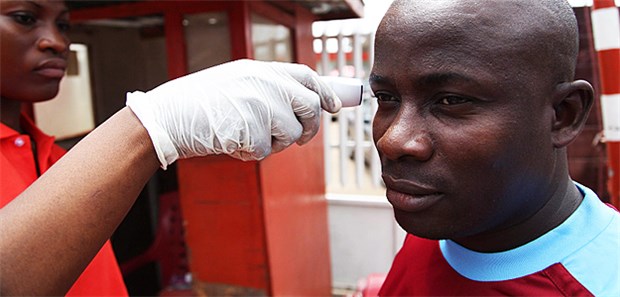
PEI-Präsident Cichutek befürwortet alle Versuche, die dazu dienen, schwerwiegende Infektionskrankheiten wie Ebola vorzubeugen.
© Ahmed Jallanzo / epa / dpa
Ärzte Zeitung: Herr Professor Cichutek, in Westafrika wütet seit Monaten das Ebola-Virus. Fast 890 Menschen sind bereits gestorben. In der Fachwelt wird der Mangel an spezifischen Therapeutika beklagt. Manche fordern gar den Einsatz ungetesteter Wirkstoff-Kandidaten. Warum gibt es bis heute eigentlich keine geeignete Therapie?
Professor Klaus Cichutek: Ebola hatte vor dem aktuellen Ausbruch nur verhältnismäßig wenige Menschenleben gefordert. Außerdem gab es nur wenige Ausbrüche, die zudem zeitlich begrenzt waren.
Die Krankheit stand deswegen nicht so sehr im Fokus der Arzneimittelentwicklung. Die Forschung muss außerdem unter Hochsicherheitsbedingungen stattfinden, wenn mit dem Ebola-Virus selbst geforscht wird, für die relativ wenige Labore gerüstet sind.
Beim jetzigen Ausbruch setzen Ärzte in Einzelfällen auf unerprobte Therapien. Jüngst wurde berichtet, ein infizierter Mediziner aus den USA, der in Westafrika gearbeitet hatte, sei mit einem Serum eines genesenen Kindes behandelt worden. Was ist davon zu halten?
Cichutek: In der jetzigen Lage sollte alles getan werden, die infizierten Patienten zu retten. Die hohe Letalität der Ebola-Viruserkrankung spricht dafür, im Rahmen von Heilversuchen alles nur Mögliche zu tun, um den Infizierten zu helfen.
Aber es handelt sich um ungeprüfte Einzeltherapien.
Dr. Klaus Cichutek

© Wolfgang Kumm / dpa
Aktuelle Position: Präsident des PEI seit Ende 2009
Ausbildung: Studium der Biochemie, Promotion 1984; Forschungsaufenthalt in Berkeley; Professor an der Goethe-Universität in Frankfurt am Main; Schwerpunkte in Retrovirologie, Gentherapie, Vektorimpfstoffen
Werdegang: Seit 1988 am PEI, Leiter der Forschergruppe „Molekularbiologie“; von 1994 bis Ende 2011 Abteilungsleiter Medizinische Biotechnologie; von Ende 2001 bis Ende 2009 Vizepräsident des PEI; Mitglied in zahlreichen Arbeitsgruppen von EMA, ICH und WHO; seit Februar 2014 Mitglied des „Product Development for Vaccines Advisory Committee (PD-VAC) der WHO“
Privates: 1956 in Recklinghausen geboren
Cichutek: Sie müssen sehen, dass es im Moment kaum laufende klinische Prüfungen von neuen Therapeutika oder Impfstoffen gibt, geschweige denn eine etablierte spezifische Behandlung. Insofern muss man zum Heilversuch greifen, den letztlich immer der Arzt vor Ort verantworten und der individuellen Situation anpassen muss.
Das Paul-Ehrlich-Institut hat hier keine Rolle. Es gibt aber durchaus wissenschaftlich publizierte experimentelle Hinweise, sowohl für Altweltaffen aber auch für Menschen beschrieben, wonach eine Ebola-Infektion mit monoklonalen Antikörpern, Blutplasma oder Seren, die hohe Antikörpertiter gegen das Ebolavirus enthalten, erfolgreich behandelt werden kann.
Insofern sind Heilversuche in angemessener Form und der Einzelsituation angepasst aus ethischer Sicht in Ordnung, wenn nicht sogar geboten. Auch Berichte über präventive Impfstoffkandidaten gibt es, die an Affen erfolgreich getestet wurden.
Sollten die Helfer vor Ort dann nicht gleich Blut von jedem genesenen Ebola-Patienten abnehmen und die daraus gewonnenen Seren zum "Masseneinsatz" verwenden?
Cichutek: Das ist illusorisch, vor allem wegen der wahrscheinlich kaum vorhandenen technischen und organisatorischen Möglichkeiten. Zudem gibt es Berichte, dass die Bevölkerung in Westafrika teilweise skeptisch gegenüber der angebotenen Hilfe ist.
Offenbar bestehen Zweifel, dass die angebotene Hilfe wirklich nützt, denn viele Infizierte sterben und Therapiemaßnahmen im späten Stadium der Infektion führen nicht mehr zum Erfolg.
Ein breit angelegter Heilversuch könnte also Ängste schüren ...
Cichutek: Eine flächendeckende, aber unkoordinierte und planlose Vorgehensweise würde uns in der jetzigen Situation nicht weiterhelfen. Auch wissen wir im Einzelfall nicht genau, wie effektiv Seren von zuvor Erkrankten in der Behandlung sein werden.
Wenn diese Seren tatsächlich von Patienten stammen, die mit demselben Virus wie der zu Behandelnde infiziert waren, virusfrei sind und die Infektion überstanden haben, stehen zumindest aus immunologischer Sicht die Chancen gut, dass die Seren eine hohe Konzentration hemmender Antikörper enthalten, was die Infektion von Patienten, die mit dem Serum behandelt werden, erfolgreich bekämpfen könnte.
Deswegen würden wir uns für einen gut durchdachten, kontrollierten Einsatz solcher Therapien aussprechen, der auch für zukünftige Ebola-Virus-Ausbrüche neue Therapieoptionen erschließt. Zu beachten sind Risiken der Übertragung anderer Krankheiten.
Seren aus Spenderblut können also höchstens im Einzelfall helfen. Wie sehen die Alternativen aus?
Cichutek: Aus Sicht des Paul-Ehrlich-Instituts ist jetzt die Gelegenheit gegeben, die klinische Erprobung neuer Therapeutika und Impfstoffe organisiert und kontrolliert voranzutreiben.
Man kann unter Umständen Menschen helfen und für die Zukunft Erkenntnisse gewinnen. Jetzt erprobt werden könnten Impfstoffkandidaten oder Antikörper-Präparationen, die nach der GMP produziert wurden oder werden können.
... der Guten Herstellungspraxis ...
Cichutek: Genau. Und Impfstoffe und Therapeutika sollten in ersten Versuchen eine gewisse Wirksamkeit gezeigt haben. Es gibt ja in der Literatur positive Berichte über mögliche Kandidaten, darunter Vektorimpfstoffe auf Adenovirus-Basis (Nature 2000; 408: 605) und auf Basis des Vesicular Stomatitis Virus (PLoS Negl Trop Dis 2013; 7(12): e2600) sowie monoklonale Antikörper oder Antikörperpräparationen gegen spezifische Ebola-Glykoproteine (Sci Transl Med 2013; 5(199): 199ra113 und Sci Rep 2013; 3: 3365).
Solche Ansätze sollen wir jetzt unter kontrollierten Bedingungen testen. Das wäre der Weg nach vorne.
Wie schnell lässt sich eine Prüfung denn auf die Beine stellen?
Cichutek: Das geht natürlich nicht ad hoc. Lassen Sie es mich so ausdrücken: Sponsoren könnten zügig eine solche Prüfung gemeinsam mit öffentlichen Mitteln, der Industrie und akademischen Einrichtungen auf die Beine stellen.
Auf diese Weise gäbe es tatsächlich Möglichkeiten, relativ schnell etwa eine klinische Prüfung zu organisieren. Das Paul-Ehrlich-Institut ist bereit, regulatorisch zu unterstützen.
Das klingt nach einem direkten Angebot an Wissenschaft und Industrie.
Cichutek: Wenn Sie so wollen, dürfen Sie das als Angebot verstehen - an die Industrie, aber auch an akademische Forscher. Das Paul-Ehrlich-Institut steht bereit. Ich kann mich dem etwa gleichlautenden Signal der amerikanischen Arzneimittelbehörde FDA nur anschließen ...
... die gesagt hatte, für Prüfungen "bereitzustehen".
Cichutek: Eine Erprobung von Therapeutika und Impfstoffen im Rahmen einer klinischen Prüfung böte einen Schutz für die Patienten, eine Aussicht auf möglicherweise erfolgreiche Behandlung und die Möglichkeit, wichtige Daten zur Sicherheit der Präparate und Wirksamkeitshinweise für zukünftige standardisierte Anwendungen zu gewinnen.
Die regulatorischen Anforderungen können von den Experten des Paul-Ehrlich-Instituts sinnvoll und trotzdem regelgerecht an die Lage angepasst werden. Wichtig im Hinblick auf eine Anwendung am Menschen wäre es, dass Daten zur Sicherheit vorliegen. Es gibt Hersteller, die die Entwicklung geeigneter Kandidaten auf dieser Basis weiter voranbringen und Fachärzte, die die klinische Prüfung begleiten könnten.
Das Paul-Ehrlich-Institut arbeitet beispielsweise als Partner des DZIF, dem Deutschen Zentrum für Infektionsforschung, an neuen Angeboten für die regulatorische Begleitung früher Arzneimittelentwicklungen. Das DZIF bereitet gerade eine klinische Phase-I-Prüfung zur Erprobung eines neuen Impfstoffes gegen ein anderes hochgefährliches Virus vor, das MERS-Coronavirus, gegen das ebenfalls weder Therapien noch Impfstoffe vorhanden sind.
Das Paul-Ehrlich-Institut erforscht in nichtklinischen Studien Chancen und Risiken von Vektor-Impfstoffen gegen das MERS-Coronavirus. So könnte auch ein neuer Impfstoff gegen Ebolavirus geprüft werden. Im DZIF gibt es klinische Prüfeinrichtungen in Deutschland und Verbindungen zu solchen Einrichtungen in Afrika, die möglicherweise für klinische Studien genutzt werden könnten.
Fehlen der Wissenschaft Anreize und Mittel, neue Therapien zu erforschen?
Cichutek: Grundsätzlich befürworte ich alle Versuche, schwerwiegenden Infektionskrankheiten vorzubeugen, diese effektiv zu behandeln und unter Umständen sogar von der Erde zu eradizieren.
Bei Ebola muss sich möglicherweise der private mit dem öffentlichen Sektor zusammentun, um alle Chancen zu nutzen. Auch Kooperationen mit der Weltgesundheitsorganisation WHO und die Arbeit der Kollaborationszentren der WHO, von denen ein Zentrum für die Impfstoffevaluation und eines für Qualität und Sicherheit von Blutprodukten hier am Paul-Ehrlich-Institut designiert sind, müssen eingebunden werden.
Kommen wir noch einmal zurück zu der klinischen Prüfung neuer Ebola-Therapien. Lassen sich diese Studien überhaupt in der jetzigen Ausbruchssituation in Westafrika durchführen?
Cichutek: Ich hatte ja angesprochen, dass es offenbar Mutmaßungen unter der dortigen Bevölkerung gibt, Afrika werde als Versuchslabor für experimentelle Therapien verwendet, die hierzulande gar nicht vertretbar seien. Diese Bedenken müssen wir ernst nehmen.
Wir könnten diesen Vermutungen unter anderem damit entgegenwirken, dass Experten und Helfern aus Europa die Teilnahme als Probanden an solche Studien angeboten wird - natürlich bei allen Teilnehmern nur nach Aufklärung und Einwilligung.
Lesen Sie dazu auch: Erste Erfolge mit Antikörper: Ebola-Experten reagieren zurückhaltend






