Lilly
Mirikizumab: Neue Option bei Colitis ulcerosa
Mirikizumab (Omvoh®) trug in Studien zu einer Remission des imperativen Stuhldrangs bei Colitis ulcerosa bei.
Veröffentlicht:
Imperativer Stuhldrang? Etwa 80 Prozent der Patienten mit Colitis ulcerosa berichten davon. Mirikizumab trug in Studien zu einer Remission des imperativen Stuhldrangs bei.
© yuriygolub / stock.adobe.com
Hamburg. Mit Mirikizumab steht Patientinnen und Patienten mit Colitis ulcerosa (CU) seit Kurzem eine neue Therapieoption zur Verfügung. Der humanisierte IgG4-Antikörper ist ein Interleukin(IL)-23p19-Inhibitor zur zielgerichteten Therapie der CU. Mit ihm lassen sich auch anspruchsvolle Therapieziele erreichen.
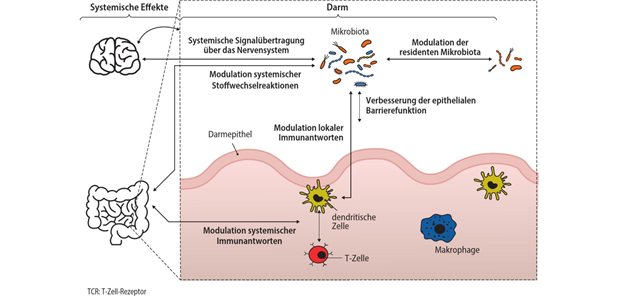
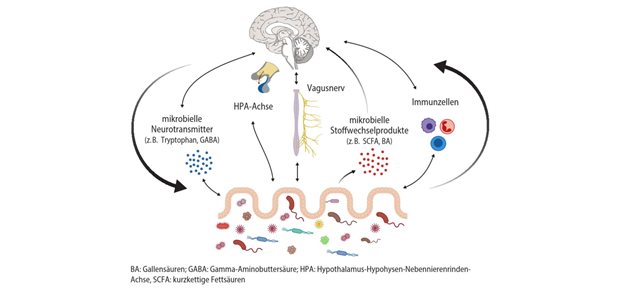
IL-23 sei das richtige Target, um modernen Therapieanforderungen gerecht werden zu können, sagte Professor Raja Atreya vom Universitätsklinikum Erlangen, der die komplexe zugrunde liegende Pathophysiologie des neuen Wirkstoffs erläuterte. Der IL-23-Signalweg spielt demnach eine wichtige Rolle in der Behandlung der CU. Und hier setzt Mirikizumab an: Es ist designt für die selektive Inhibition von IL-23 durch die hochaffine Bindung an die Untereinheit p19 und kann somit den Teufelskreis der Inflammation durchbrechen. Anspruchsvolle Therapieziele sind mit dem ersten Interleukin-23p19-Inhibitor bei Colitis ulcerosa schnell und anhaltend erreichbar.
HERM und BU-Remission erreichbar
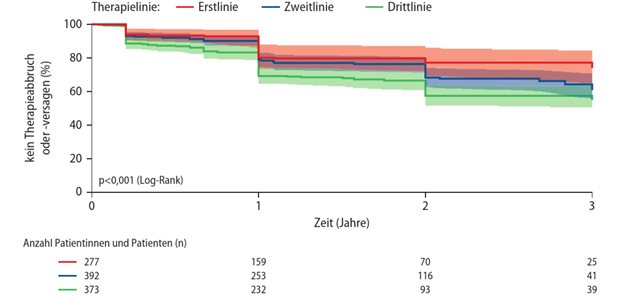
In den Zulassungsstudien LUCENT-1 und LUCENT-2 richtete sich der Blick nicht nur auf die klinische Remission, sondern auch auf neue, ambitionierte Therapieziele wie die HEMR (histologisch-endoskopische Schleimhautremission) und die Bowel-Urgency (BU)-Remission. Die HEMR wird dabei als strikter und innovativer Kombinationsendpunkt von mehr als 40 Prozent der Patientinnen und Patienten nach 52 Behandlungswochen erreicht.
Auch der imperative Stuhldrang wird günstig beeinflusst. Unter Mirikizumab (Omvoh®) erreichten die Patientinnen und Patienten im Vergleich zu Placebo in Woche 12 und in Woche 40 signifikant häufiger eine BU-Remission (LUCENT-1: 22,1 Prozent versus 12,3 Prozent; LUCENT-2: 42,9 versus 25 Prozent). Von imperativem Stuhldrang sind ja etwa 80 Prozent der Patientinnen und Patienten betroffen, mehr als die Hälfte sogar täglich.
Die überzeugenden Ergebnisse für Mirikizumab in den Zulassungsstudien bestätigten sich auch in der klinischen Anwendung, berichtete Dr. Lars Fechner, niedergelassener Gastroenterologe aus Halle/Saale, über seine ersten Erfahrungen mit Mirikizumab. Sie zeigen „eine mindestens so überzeugende Wirksamkeit wie in den LUCENT-Studien“. (feb)
Quelle: Launch-Fachpressekonferenz Omvoh® (Mirikizumab), Hamburg, September 2023; Veranstalter: Lilly