US-Studie zu ChAdOx1-S
AstraZeneca räumt leicht geringere Wirksamkeit von Corona-Vakzine ein
Nach Zweifeln der US-Behörde NIAID an ursprünglich publizierten Daten hat AstraZeneca die Effektivität seines COVID-Impfstoffs korrigiert – leicht nach unten.
Veröffentlicht: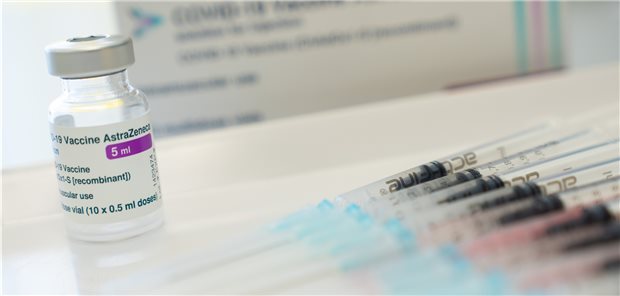
Aufgezogene Spritzen mit ChAdOx1-S in einer Hausarztpraxis in Bayern: In einer Phase-III-Studie in Amerika erreichte die Vakzine eine relative Risikoreduktion von 76 Prozent.
© Nicolas Armer / dpa
Cambridge. AstraZeneca hat die vorläufigen Wirksamkeitsdaten seiner COVID-Vakzine ChAdOx1-S (AZD1222) aus der noch andauernden Phase-III-Studie in Amerika leicht nach unten korrigiert. Nachdem das Unternehmen am Montag den Schutz der Impfung gegen symptomatische COVID-19 in der Studie mit 79 Prozent angegeben hatte, bezifferte es den Effekt am Donnerstag in einer neuen Mitteilung mit 76 Prozent.
Die Wirksamkeit (in Form der relativen Risikoreduktion, RRR) gegen schwere Verläufe und Hospitalisierung wegen COVID-19 wird weiter mit 100 Prozent angegeben, ebenso wie die 85-prozentige Effektivität gegen symptomatische Corona-Infektionen bei Senioren ab 65 Jahre.
Die Ergebnisse seien inzwischen mit dem unabhängigen „Data Safety Monitoring Board“ (DSMB) abgestimmt worden, so das Unternehmen. Für die am Montag vorgestellten Resultate habe man 141 Erkrankungen berücksichtigt, die bis zum 17. Februar unter den über 32 .000 Studienteilnehmern aufgetreten waren.
Kritik nach erster Pressemitteilung
Für die neue aktuellere Analyse habe man jetzt 190 Erkrankte berücksichtigt. Die neue Auswertung bestätige dabei die positiven „high-level“-Ergebnisse, so AstraZeneca.
Nach der Pressemeldung am Montag hatte das DSMB Zweifel an den vom Unternehmen publizierten Daten angemeldet. Das US-National Institute for Allergy and Infectious Diseases (NIAID) hatte daraufhin in einer ungewöhnlichen Stellungnahme AstraZeneca dazu aufgefordert, gemeinsam mit dem DSMB die Daten zu sichten und so genau wie möglich die aktuellsten Wirksamkeitsbelege zu veröffentlichen.
Das Unternehmen braucht die Studie mit Probanden aus den USA, Chile und Peru für einen Zulassungsantrag bei der US-Arzneibehörde FDA. Weil die Zulassung in den USA bisher fehlt, kann mit der Vakzine dort noch nicht geimpft werden. (eis)