Kardiologe warnt vor Panik
Verunreinigtes Valsartan – kein Krebsscreening nötig
Trotz Verunreinigung von Valsartan-Präparaten mit dem potenziell krebserregenden Stoff NDMA sieht der Kardiologe Professor Thomas Meinertz derzeit keinen Grund für ein Krebsscreening bei betroffenen Patienten. Zum künftigen Schutz plädiert er für eine Bundesbehörde für Arzneikontrollen.
Veröffentlicht: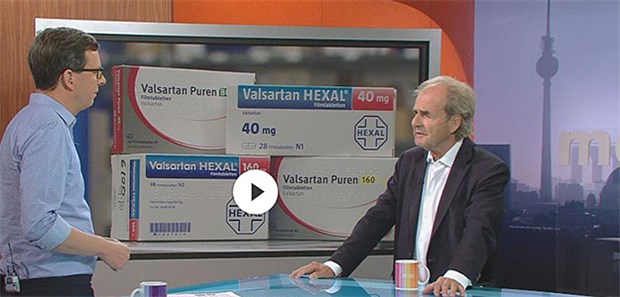
Valsartan-Rückruf: Prof. Thomas Meinertz (r.) äußerte sich im ZDF MoMa dazu, was Patienten beachten müssen.
© Screenshot ZDF Morgenmagazin-Sendung vom 31.7.2018
BERLIN. Es ist eine der größten Arzneimittelrückrufaktionen in Deutschland: 17 Firmen mussten bislang größere Mengen an Valsartan-Präparaten zurückrufen.
Die betroffenen Blutdrucksenker könnten mit N-Nitrosodimethylamin, kurz NDMA – einer potenziell krebserregenden Substanz, verunreinigt sein.
Zudem rief das Unternehmen Hormosan seinen Blutdrucksenker Irbesartan vorsichtshalber teilweise aus den Apotheken zurück, wegen möglicher NDMA-Verunreinigungen.
Nach aktuellem Stand könnten allein im letzten Jahr zirka 900.00 Patienten verunreinigte Medikamente eingenommen haben.
Hilfe für betroffene Valsartan-Patienten
In einem aktuellen Beitrag im ZDF Morgenmagazin bekräftige nun der Kardiologe Professor Thomas Meinertz, ehemaliger Vorstand der Herzstiftung, dass Patienten, die betroffene Präparate (siehe Kasten am Textende) erhalten haben, diese sofort absetzen sollten – allerdings nur mit ärztlicher Unterstützung.
Ärzte sollten ihren Patienten dann entweder ein Valsartan-Präparat eines nicht betroffenen Herstellers, ein anderes Sartan oder einen gänzlich anderen Blutdrucksenker verordnen – bei der Vielzahl vorhandener Alternativen sei das auch kein Problem.
Für den Fall einer Umstellung auf einen anderen Vertreter der Sartanklasse hat zum Beispiel die Arzneimittelkommission der Apotheker (AMK) eine Tabelle mit Äquivalenzdosierungen veröffentlicht.
"Valsartan-Patienten müssen nachbeobachtet werden"
Ob sich konkrete gesundheitliche Risiken durch die mitunter langjährige Einnahme von Valsartan bei einzelnen Patienten ergeben haben, sei "ganz schwer abschätzbar", sagte Meinertz.
Inzwischen ist zumindest klar: NDMA könnte bereits 2014, eventuell sogar schon früher, in Umlauf gekommen sein. Erste toxikologische Untersuchungsdaten betroffener Präparate hat die AMK kürzlich vorgestellt.
Das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) weist allerdings darauf hin, dass für eine konkrete Bewertung gesundheitlicher Risiken noch validierte Prüfverfahren fehlten.
Auch Meinertz betont, man werde wohl die Patienten nachbeobachten müssen. Dennoch gebe es keinen Anlass für Panik. Auch für ein ausgedehntes Krebsscreening sieht er derzeit keinen Anlass.
Produktionsumstellung bei chinesischem Hersteller mit NDMA-Resten
Schuld am Valsartan-Skandal ist offenbar eine Produktionsumstellung beim chinesischen Hersteller Zhejiang Huahai Pharmaceutical, wie die Europäische Arzneimittelbehörde EMA berichtet. Demnach falle nach der Umstellung im Jahr 2012 bei einem Produktionszwischenschritt NDMA an, das dann offenbar nicht konsequent wieder entfernt worden sei.
Enthalten seien zwar nur geringste Mengen im Nanogramm-Bereich, aber es handle sich immerhin um einen potenziell – wohl auch für Menschen – krebserregenden Stoff, erinnerte Meinertz in dem Fernsehbeitrag.
Seiner Ansicht "liegt ein Fehler im System" vor, der dazu führte, dass die Verunreinigungen so lange nicht entdeckt wurden. Aus historischen Gründen seien Landesbehörden für die Kontrolle zuständig und die "sind damit völlig überfordert", wie man an diesem Beispiel sehe, kritisierte der Kardiologe.
Dass jahrelang offenbar keine Kontrolluntersuchungen stattfanden, kann Meinertz nicht verstehen. "Das muss dringlich geändert werden, zum Beispiel durch eine Bundesbehörde, die die Einfuhr stichprobenhaft auf Verunreinigungen kontrolliert", forderte er. (run)
Zurückgerufene Valsartan-Präparate
Die nachfolgenden Valsartan-haltigen Arzneimittel sind laut Arzneimittelkommission der Deutschen Apotheker (AMK) vom Rückruf betroffen:
• Valsartan - 1 A Pharma 40, 80, 160 und 320 mg, 28, 56 und 98 Filmtabletten, Valsartan - 1 A Pharma plus 80/12,5, 160/12,5, 160/25, 320/12,5 und 320 mg/25 mg, 28, 56 und 98 Filmtabletten
• Valsartan AAA 40, 80, 160 und 320 mg, alle Packungsgrößen, Filmtabletten
• Valsargamma 80 mg, alle Packungsgrößen, Filmtabletten (Ergänzung)
• Valsartan AbZ 40, 80, 120, 160, 320 mg, Valsartan comp. AbZ 80/12,5, 160/12,5, 160/25, 320/12,5, 320 mg/25 mg, Valsartan CT 120, 160 mg, Valsartan comp.-CT 80/12,5, 160/12,5, 160/25 und 320 mg/25 mg, Filmtabletten
• Valsartan-Actavis 80 mg, 28 Filmtabletten, Valsartan-Actavis 320 mg, 28, 56 und 98 Filmtabletten
• Valsartan AL 40 mg, 28 Filmtabletten, Valsartan AL 80, 160 und 320 mg, 98 Filmtabletten, Valsartan/HCT AL 160/12,5, 160/25, 320 mg/25 mg, 98 Filmtabletten
• Valsartan AL 40 mg, 28 Filmtabletten (Ergänzung)
• Valsartan comp Basics 80/12,5, 160/12,5 und 160 mg/25 mg, 28, 56 und 98 Filmtabletten
• Valsartan Dexcel 80 und 160 mg, 98 Filmtabletten
• Valsartan Hennig 40, 80, 160 und 320 mg, alle Packungsgrößen, Filmtabletten, Valsartan Hennig plus HCT 80/12,5, 160/12,5, 160/25, 320/12,5 und 320 mg/25 mg, alle Packungsgrößen, Filmtabletten
• Valsartan Heumann 40, 80, 160 und 320 mg, 28, 56 und 98 Filmtabletten
• Valsartan Hexal® 40 mg, 28 Filmtabletten, Valsartan Hexal® 80, 160 und 320 mg, 28, 56 und 98 Filmtabletten, Valsartan Hexal® comp 80/12,5, 160/12,5, 160/25, 320/12,5 und 320 mg/25 mg, 28, 56 und 98 Filmtabletten
• Valsartan-Hormosan comp 80/12,5, 160/12,5 und 160 mg/25 mg 28 und 98 Filmtabletten
• Valsartan Puren, 40, 80, 160 und 320 mg, alle Packungsgrößen, Filmtabletten, Valsartan Puren 80/12,5, 160/12,5, 160/25, 320/12,5 und 320 mg/25 mg, alle Packungsgrößen, Filmtabletten
• Valsartan-ratiopharm® 40, 80, 120, 160 und 320 mg, alle Packungsgrößen, Filmtabletten, Valsartan-ratiopharm® comp. 80/12,5, 160/12,5, 160/25, 320/12,5 und 320 mg/25 mg, alle Packungsgrößen, Filmtabletten
• Valsartan Stada 40, 80, 160 und 320 mg, 28, 56 und 98 Filmtabletten, Valsartan/HCT Stada 80/12,5, 160/12,5 und 320 mg/25 mg, 98 Filmtabletten, Valsartan/HCT Stada 160 mg/25 mg, 28 und 98 Filmtabletten
• Valsartan Zentiva 40, 80, 160 und 320 mg, alle Packungsgrößen und Valsartan Zentiva comp. 80/12,5, 160/12,5, 160/25, 320/12,5 und 320 mg/25 mg, alle Packungsgrößen