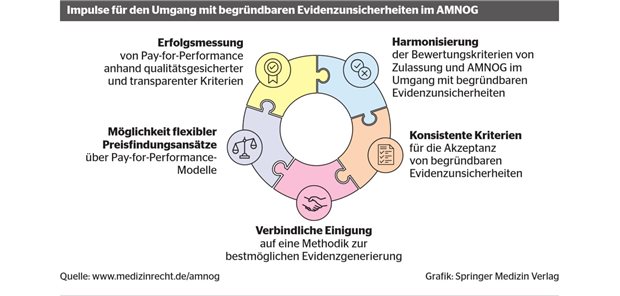
Herausforderungen für die künftige Nutzenbewertung
Hecken: Früh das Evidenzniveau neuer Wirkstoffe verbessern!
Der Umgang mit dem Evidenzniveau etwa bei Orphan Drugs, die anwendungsbegleitende Datenerhebung und die frühe Etablierung von Registern gehören zum künftigen Aufgabenportfolio des GBA beim AMNOG.
Veröffentlicht:Das AMNOG-Verfahren „ist eine feste Größe auf dem Weg in den Arzneimittelmarkt Deutschlands“, resümiert der Vorsitzende des Gemeinsamen Bundesausschusses,(GBA) Professor Josef Hecken. Primär als Instrument zur fairen Preisgestaltung gedacht, führe das Gesetz in der „Konsequenz zu einer unabhängigen, evidenzbasierten Arzneimittelbewertung – ohne vierte Hürde“.
Drei Herausforderungen definiert Hecken für die Zukunft: Den Umgang mit abnehmendem Evidenzniveau bei den regulatorisch priorisierten Arzneimitteln, Orphan Drugs und beschleunigten Zulassungen.
Neben Arzneimitteln, deren tatsächlicher beachtlicher Therapieerfolg in sauber durchgeführten Studien nachgewiesen seien, stünden aber Medikamente, bei denen nicht bekannt sei, ob der erhoffte Erfolg eintrete.
Medical Need statt Evidenz?
Dabei stünden Zulassungsbehörden unter einem „enormen Druck“ von Industrie, Medizin, Patienten und Politik, Zulassungen noch schneller zu erteilen und Evidenzansprüche zu senken. Die Zeitersparnis gehe auf Kosten valider Daten und gesicherter Endpunkte.
Zulassungsentscheidungen, die mehr durch das Argument des Medical Need und weniger auf Basis von Evidenz getroffen werden, machten auch die Bewertung des Zusatznutzens schwieriger.
Lösen lassen sich einige Probleme nach Heckens Auffassung durch das Instrument der anwendungsbegleitenden Datenerhebung. Mit gut geplanten Registerstudien sei es möglich, Daten zu bestimmten patientenrelevanten Endpunkten zu generieren. Allerdings lasse sich damit das Problem fehlender Vergleichsdaten nicht lösen.
Dateninterpretation größte Herausforderung
Deshalb sei es erforderlich, bereits während der Arzneimittelentwicklung – also vor der Zulassung – an Registern zu arbeiten. Eine frühzeitige Konzeption der Datenerhebung , um Krankheitsverläufe zu erfassen, „wäre wünschenswert“.
Hecken: „Die Interpretation der nach der Nutzenbewertung erhobenen Daten mit Augenmaß, aber auch mit gleichem Maßstab zu bewerten, wird eine der größten Herausforderungen der nächsten Jahre werden.“
Von zunehmender Bedeutung werde die europäische HTA-Zusammenarbeit. Noch sei unklar, wie bei einem harmonisierten europäischen HTA-Verfahren Studien bewertet werden und welches gemeinsame Verständnis von der Qualität einzureichender Daten gelten solle. Notwendig sei daher vor der endgültigen Implementierung eine Testphase. (HL)