COPS-Studie / ESC-Kongress
Colchicin für Herzinfarkt-Patienten? Warum die Gene entscheidend sein könnten
In der Studie COPS konnte Colchicin die Effektivität, die es bei Myokardinfarkt-Patienten bereits gezeigt hatte, teilweise replizieren. Eine Analyse deutet zudem an, dass die Entscheidung für eine solche antiinflammatorische Sekundärprävention auf Basis der Gene gefällt werden sollte.
Veröffentlicht:
Die chemische Struktur von Colchicin. Kardiologen prüfen das Potenzial der Substanz für ihre Patienten.
© Zerbor / stock.adobe.com
Sophia Antipolis. Das alte Gichtmittel Colchicin hat einen Lauf. Das entzündungshemmende und immunmodulierende Medikament macht nicht nur bei kardiologischen Indikationen auf sich aufmerksam. Es wird derzeit in der internationalen COLCORONA-Studie auch als Frühtherapie bei COVID-19-Erkrankung evaluiert.
Beim digitalen ESC-Kongress 2020 stellte der Kardiologe Professor Jamie Layland von Ramsay Health Care in Frankston, US-Bundesstaat Victoria, die COPS-Studie vor, die Colchicin – ähnlich wie die COLCOT-Studie – nach Myokardinfarkt im Hinblick auf künftige kardiovaskuläre Ereignisse evaluiert hat.
Im Test bei Infarktpatienten
An der COPS-Studie nahmen 795 Patienten mit akutem Koronarsyndrom teil, sie war also kleiner als die COLCOT-Studie mit ihren über 4700 Teilnehmern. Primärer Endpunkt war ein Komposit aus Tod, akutem Koronarsyndrom, Schlaganfall oder ischämiebedingter Revaskularisierung.
Behandelt wurde mit Colchicin 0,5 mg zweimal täglich für vier Wochen, danach 0,5 mg einmal täglich für elf Monate oder entsprechende Placebozubereitungen zusätzlich zu einer optimalen sonstigen medikamentösen Therapie. Die Studienpatienten hatten überwiegend einen STEMI oder NSTEMI, 87 Prozent wurden per perkutaner Intervention behandelt. Kardiovaskuläre Folgeereignisse waren insgesamt selten.
Trend stimmt, Signifikanz verfehlt
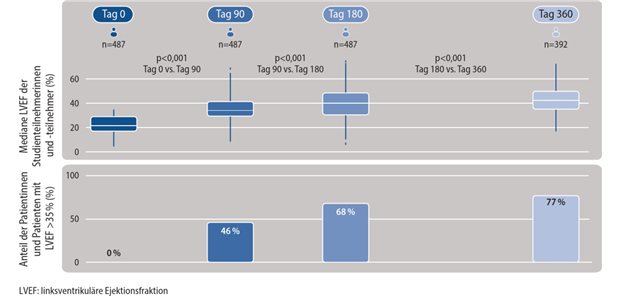
In dem für den primären Endpunkt relevanten 12-Monats-Follow-up gab es einen Trend zugunsten des Colchicins, der das Signifikanzniveau aber verfehlte (p=0,09). Das änderte sich mit etwas längerem Follow-up. Schon bei der 400-Tage-Auswertung war die Intention-to-Treat-Analyse zugunsten des Colchicins signifikant. Der Unterschied war getrieben durch eine Verringerung von akuten Koronarsyndromen, Schlaganfällen und Revaskularisationen. Todesereignisse waren im Colchicin-Arm der Studie häufiger.
Deutlich günstiger sieht die Per-Protocol-Analyse aus. Hier hatten Colchicin-Patienten eine Risikoreduktion um 58 Prozent (p=0,01).
Bei der virtuellen ESC-Tagung diskutierten Layland und Dr. Massimo Imazio von der Universität Turin mögliche Gründe für die Unterschiede zur COLCOT-Studie. Ein Grund speziell für die nicht signifikante Intention-to-Treat-Analyse könnte demnach sein, dass Colchicin in den ersten vier Wochen doppelt so hoch dosiert wurde wie in der COLCOT-Studie, die durchweg mit 0,5 mg einmal täglich gearbeitet hatte. Die Unterschiede bei den Todesereignissen führten die Experten auf die kleine Studiengröße zurück. Die Studie war nicht für Mortalität gepowert.
Warum manche Patienten zu Nebenwirkungen neigen
Ebenfalls vorgestellt wurden beim virtuellen ESC-Kongress die Ergebnisse einer pharmakogenetischen Subanalyse der COLCOT-Studie, an der immerhin 1656 von 4745 COLCOT-Patienten teilgenommen hatten. Dabei wurden insgesamt drei Genloci identifiziert, die für die (bei einigen Patienten stark nebenwirkungsbehaftete) Colchicin-Behandlung von Bedeutung zu sein scheinen. So gibt es ein Gen auf Chromosom 9, das an der Mikrotubuli-Stabilisierung beteiligt ist und bei dem ein relativ häufiges Allel mit einer besseren Colchicin-Wirkung einhergeht. Das ist auch funktionell plausibel, denn Colchicin wirkt wahrscheinlich (auch) über eine Hemmung der Mikrotubulus-Bildung.
An zwei weiteren Genorten auf den Chromosomen 6 und 10 sind bestimmte Risikoallele mit einem höheren Risiko für gastrointestinale Nebenwirkungen assoziiert. „Insgesamt sprechen diese Ergebnisse für eine künftige, personalisierte Herangehensweise an die antiinflammatorische Behandlung in der kardiovaskulären Sekundärprävention“, resümierte Professor Marie-Pierre Dubé von der Universität Quebec.