EvidenzUpdate-Podcast
Hoffnung und Kollaps – wie Lecanemab uns herausfordert
Ein Antikörper wird zur Hoffnung gegen Alzheimer-Demenz. Was bringt er wirklich? Ein EvidenzUpdate darüber, wie wir mit ihm umgehen sollten – und wie sich ein Versorgungs-Overkill verhindern lässt.
Veröffentlicht:
Der Protofibrillen-Antikörper Lecanemab gegen Beta-Amyloid-Ablagerungen ist für viele eine große Hoffnung. Sobald er formal zugelassen ist, wird er die erste zielgerichtete Therapie bei Morbus Alzheimer sein. In der randomisiert-kontrollierten Zulassungsstudie Clarity AD mit 18-monatigem Beobachtung hat er im Mittel zu einer sechsmonatigen Progressionsverzögerung gegenüber Placebo geführt. Allerdings: Nicht nur die Anwendung ist aufwändig (Infusion über mindestens eine Stunde, mehrfache MRT-Kontrollen), auch das Case-Finding hat es in sich.
Wir schauen uns die Ergebnisse aus der Phase-3-Studie – und den Appendix – genauer an und stellen die Frage, was klinisch relevant ist. Wir überlegen, welche Personen von der Antikörper-Therapie profitieren könnten, wie eine Versorgungskette aussehen würden und was das für die Versorgung in toto bedeuten würde. Spoiler: Es gibt auch ein paar ökonomische Überlegungen. (Dauer: 30:56 Minuten)
Anregungen? Kritik? Wünsche?
Schreiben Sie uns: evidenzupdate@springer.com
Shownotes
- Schudok A. EMA empfiehlt Zulassung von Alzheimer-Mittel Lecanemab nun doch. Ärzte Zeitung. 2024. www.aerztezeitung.de (accessed 4 Dec 2024).
- Leqembi | European Medicines Agency (EMA). www.ema.europa.eu. 2024. www.ema.europa.eu (accessed 4 Dec 2024).
- van Dyck CH, Swanson CJ, Aisen P, et al. Lecanemab in Early Alzheimer’s Disease. New England Journal of Medicine 2022;388:9–21. doi: 10.1056/nejmoa2212948
- Swanson CJ, Zhang Y, Dhadda S, et al. A randomized, double-blind, phase 2b proof-of-concept clinical trial in early Alzheimer’s disease with lecanemab, an anti-Aß protofibril antibody. Alzheimer’s Research & Therapy 2021;13. doi: 10.1186/s13195-021-00813-8
- Linus Jönsson, Anders Wimo, Handels R, et al. The affordability of lecanemab, an amyloid-targeting therapy for Alzheimer’s disease: an EADC-EC viewpoint. The Lancet regional health 2023;29:100657–7. doi: 10.1016/j.lanepe.2023.100657
- Mahase E. NICE rejects Alzheimer’s drug donanemab owing to cost and ‚significant health risks’. BMJ 2024;387:q2342–2. doi: 10.1136/bmj.q2342
- Ebell MH, Barry HC, Baduni K, et al. Clinically Important Benefits and Harms of Monoclonal Antibodies Targeting Amyloid for the Treatment of Alzheimer Disease: A Systematic Review and Meta-Analysis. Annals of Family Medicine 2024;22:50–62. doi: 10.1370/afm.3050
- EISAI’S APPROACH TO U.S. PRICING FOR LEQEMBITM (LECANEMAB), A TREATMENT FOR EARLY ALZHEIMER’S DISEASE, SETS FORTH OUR CONCEPT OF ‚SOCIETAL VALUE OF MEDICINE’ IN RELATION TO ‚PRICE OF MEDICINE’ | News Release:2023. Eisai Co., Ltd. 2023. www.eisai.com (accessed 4 Dec 2024).
- Blotenberg I, Hoffmann W, Jochen René Thyrian. Dementia in Germany: epidemiology and prevention potential. Deutsches Arzteblatt International 2023;120:470–6. doi: 10.3238/arztebl.m2023.0100
- Deep Dive: Starten bald die ersten Lecanemab-Therapien? DGN. 2024. dgn.org (accessed 4 Dec 2024).
Transkript
Nößler: Eine Pille gegen das Vergessen – wie großartig wäre das denn? Und wenn sie auch noch ein Morbus Alzheimer aufhalten könnte, das wäre wohl phänomenal. Nur, was wollen wir uns so was eigentlich kosten lassen? Dazu gehen wir heute auf Spurensuche. Und damit herzlich willkommen zu einer neuen Episode des EvidenzUpdate-Podcast. Wir, das sind ...
Scherer: Martin Scherer.
Nößler: Präsident der Deutschen Gesellschaft für Allgemeinmedizin und Familienmedizin der DEGAM und Direktor des Instituts und Poliklinik für Allgemeinmedizin am UKE in Hamburg. Und hier am Mikrofon ist Denis Nößler, Chefredakteur der Ärzte Zeitung aus dem Haus Springer Medizin. Moin nach Hamburg, Herr Scherer!
Scherer: Moin nach Neu-Isenburg, Herr Nößler.
Nößler: Ja, so ist das. Die Fans unter uns werden es wissen. Sie haben ja nicht nur ein Institut am UKE und eine Poliklinik, Sie haben auch eine Ambulanz am UKE, eine allgemeinmedizinische. Wir wollen heute über Alzheimer – ich hatte es schon gesagt – sprechen und über jüngste Entwicklungen. Vielleicht mal so Bauchgefühl: Wie häufig kommt in einem Beratungsanlass Pi mal Daumen das Thema Gedächtnisstörung vor, Gedächtnisprobleme, Erinnerungsprobleme?
Scherer: Also bei den Älteren sind es ungefähr 40 Prozent, die davon betroffen sind.
Nößler: Also Ältere so ab 60, 65. Dann kann sich jeder da draußen schon mal so eine Größenordnung auch gesellschaftsmäßig vorstellen. Wir reden heute über Amyloid-beta-Antikörper zur Behandlung bei Morbus Alzheimer. Die meisten haben es mitbekommen, dass es konkret für Lecanemab, Handelsname ist Leqembi, eine Zulassungsempfehlung gibt vom CHMP der EMA, ausgesprochen am 14. November. Interessant dabei ist, dass der CHMP erst mal Anfang des Jahres dagegen votiert hat. Dann gab es noch mal einen Antrag, jetzt haben sie dafür gestimmt. Und wir wollen uns ein bisschen damit beschäftigen, was das ist und vor allem, was es bedeuten würde, wenn das in die Versorgung kommt. Und vielleicht, Herr Scherer, können wir erst mal so ein bisschen in diese Zulassungsdaten schauen. Die Studie heißt Clarity AD, ist eine Phase-III-Studie. Was wissen wir daraus zu Lecanemab?
Scherer: Bei Clarity ist es so wie bei eigentlich allen Studien, die wir hier besprechen. Es gibt Stärken uns Schwächen. Also die Clarity-Studie hat Hinweise dafür geliefert, dass bei Patientinnen und Patienten mit frühbeginnender Alzheimerdemenz und einem vorhandenen Amyloid-Plaque-Befall eine Verzögerung der Krankheitsprogression zu beobachten ist. Das ist ja das, was wir uns wünschen: ein Medikament in der Hand, das wirksam ist bei Alzheimer. Auch hier die Schwierigkeit natürlich, dass es sich um Frühstadien handelt, Sie haben es eben angesprochen, Herr Nößler, das bringt sicherlich Probleme bei der Patientenselektion.
Nößler: Genau. Frühstadien heißt, man muss sie früh rausfischen. Da sprechen wir gleich noch mal drüber. Ich würde gerne noch ein bisschen in den Ergebnissen der Arbeit bleiben. Herr Scherer, es ist Placebo-kontrolliert, ist verblindet gewesen, ganz ordentliche kontrollierte Studie. 18 Monate lief die. Das heißt, wir können im Prinzip im Moment erst mal nur über 18 Monate blicken. Und man sieht tatsächlich, dass alle möglichen Scores fallen. Und es sind wahnsinnig viele Scores. Was nehmen wir daraus mit, wenn wir uns das angucken? Lesetipp Seite 14.
Scherer: Der primäre Endpunkt der Studie war die Veränderung des Clinical Dementia Rating Sum of Boxes (CDR-SB). Das ist schon ein etabliertes Maß zur Beurteilung der kognitiven und funktionellen Beeinträchtigung. Und der Endpunkt ist auch klinisch relevant, weil es da natürlich um die Auswirkungen auf das tägliche Leben der Patienten geht. Es gibt sekundäre Endpunkte, wie die Messung der Amyloid-Reduktion durch PET-Scans und die Beurteilung der kognitiven Funktionen wie zum Beispiel Mini Mental State Examination, den kennt man, das ist der MMSE. Also das sind erst mal solide Ansätze.
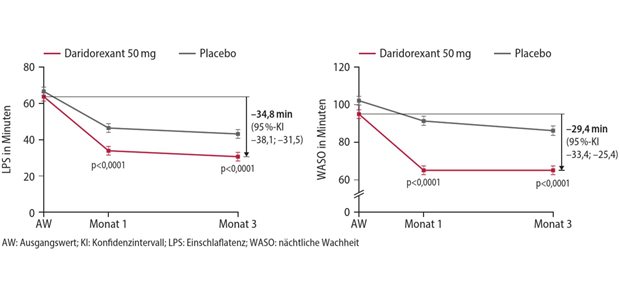
Nößler: Dann guckt man rein und sieht, von Baseline ist dann immer irgendwie null, sind dann quasi zwei Linien, nämlich der Verum-Arm und der Placebo-Arm, die sich unterschiedlich entwickeln. Diesen CDRSB, den Sie jetzt gerade als doch valides Mittel bezeichnet haben, irgendwie auf null bis 18 wird das aufgetragen, dann werden quasi Mean Changes verglichen im Verlauf von 18 Monaten. Und am Ende stellt man fest, dass der Unterschied 0,45 Punkte beträgt. Das heißt, unter Placebo ist es um 0,45 Punkte mehr abgefallen dieser Score als unter Lecanemab – von 18. Was ist das für eine Größenordnung? Sie sagten klinisch relevant.
Scherer: Das eine ist natürlich, dass das CDR-SB nicht alle Aspekte der Alzheimerkrankheit betrifft. Und dann sind diese Punkte in er Skala nicht so, dass man sagen: Hier ändert sich etwas Grundlegendes am Alltag.
Nößler: Ich will es noch mal anders machen: Man kann ja schauen, wie sich diese zwei Linien, wenn wir jetzt nur mal bei der bleiben, das kann man mit den anderen Scores, die da ermittelt wurden, es wurde auch das Amyloid gemessen, Amyloid Burden im PET. Aber man kann ja für alle diese Linien gucken, wann würden die sich wie kreuzen. Also im Prinzip eine Art Progressionsverzögerung. Und wenn man sich das bei dem CDR-SB anschaut, dann kommt man relativ gut darauf, dass die Antikörpergabe eigentlich sechs Monate rauszögert. Das heißt, ich bin mit dem Antikörper in sechs Monaten genau dort, wo ich ohne Antikörper sechs Monate vorher war, oder?
Scherer: Das ist einfach die eine Abbildung, auf Seite 14, meinen Sie?
Nößler: Genau, richtig.
Scherer: Da liegt Lecanemab deutlich über Placebo. Und das hat man immer ganz oft bei diesen Kurven. Die starten dann gemeinsam und driften dann so scherenartig auseinander. Und was Sie jetzt gemacht haben, ist, eine Linie zu ziehen von Lecanemab nach 18 Monaten, dann nach links auf der x-Achse und dann schneiden sie den Placeboeffekt sechs Monate vorher. Und dann kommen sie eben auf diese Progression. Mit anderen Worten: Nach einem halben Jahr ist man auch da, wo man ohne das Medikament wäre. Und das bei doch erheblichen Kosten und natürlich auch mit Nebenwirkungen.
Nößler: Kosten, da reden wir gleich noch mal und Nebenwirkungen. Ich will noch mal das Thema klinische Relevanz ansprechen. Ohne dass wir heute zu tief in diese einzelnen Scores einsteigen wollen, es sind erheblich viele Scores gecheckt worden. Es gibt auch systematische Reviews dazu, die diese ganzen Arbeiten, unter anderem auch diese Arbeiten, sich angeschaut haben. Herr Scherer, ich würde sagen, wir verlinken das alles. Das machen wir wo?
Scherer: In den Shownotes.
Nößler: Und dieser eine Review, den wir da jetzt mal reinpacken, der hat, wie gesagt, verschiedene Arbeiten sich angeguckt, auch die zu Lecanemab. Da ist dann auch noch Aducanumab dabei, Donanemab. Donanemab steht auch in den Startlöchern für eine Zulassung. Aducanumab hat zurückgezogen. Das ist alles ähnlich. Und da in dem Review heißt es, dass none of the changes of clinical relevance hätten. Also es gibt doch dann dieses Stichwort MCID. Was ist das? Ich vergesse das immer. Minimum Clinical Important Difference.
Scherer: Ja, genau.
Nößler: Wann ist denn etwas sinnvollerweise für Sie eine klinisch wichtige Entscheidung? Wenn wir mal beim Thema Demenz bleiben. Was wäre für Sie ein relevanter Endpunkt, den wir uns angucken müssten, den wir untersuchen müssten, damit wir irgendwann sagen können: Das bringt es oder eben nicht.
Scherer: Die Minimum Clinical Important Difference ist eine Maßzahl, die angibt, welche Veränderungen in einem klinischen Parameter für den Patienten als signifikant noch angesehen wird, um eine Verbesserung seines Gesundheitszustands wahrzunehmen oder um eine Änderung in der Behandlung zu rechtfertigen. Im Grunde genommen zeigt diese Difference an, hier ist eine Indikation, mit der ich auch eine relevante Verbesserung für den Patienten machen kann.
Nößler: Und das könnte man jetzt mit diesen Scores machen, diese Minimal Difference anlegen. Noch mal ein bisschen einfacher gesprochen: Was wäre für Sie ein sinnvoller klinischer Endpunkt, den wir messen sollten, um herauszufinden, ob solche Antikörper uns irgendein Benefit bringen? Ist es am Ende nur ein Score? Oder was würden Sie eigentlich messen wollen?
Scherer: Ein primäres Ziel, gerade bei der Alzheimer-Behandlung ist es, die Lebensqualität der Patienten zu erhalten. Und wir wissen auch, dass eine Verzögerung des kognitiven Abbaus dann dabei helfen kann, im Alltag besser zu funktionieren. Und das wiederum wirkt sich auf die Lebensqualität aus, weil die unterschiedlichen Funktionskapazitäten dann einfach verbessert werden. Wir kennen es aus dem SF-36 beispielsweise, die soziale Rollenfunktion, die emotionale Rollenfunktion. Gerade diese Exekutivfunktionen, die sind im Grunde genommen der Dreh- und Angelpunkt der Lebensqualität. Wenn die nicht funktionieren, dann kann ich mich nicht verabreden, dann habe ich keine soziale Teilhabe, dann klappt es mit dem Haushalt nicht mehr, dann kann ich mir kein Essen kochen. Also da hängt eigentlich ein Großteil der Lebensqualität dran.
Nößler: Hier an der Stelle vielleicht ein Zwischenfazit von Martin Scherer. Wenn ich Sie richtig verstehe, sagen Sie: Ja, wir sehen in dieser Arbeit, dass da was passiert, dass da auch erheblich kleine Dinge sich verbessern. Im Moment nur kurz, sechs Monate, das ist das, was wir wissen. Aber eigentlich müssten wir jetzt noch eine weitere Arbeit machen, die sehr viel länger, beispielsweise mit SF-36, untersucht, welchen Impact hat es auf deinen Alltag.
Scherer: So ist es. Und dann gibt es natürlich auch noch so ein paar methodische Einschränkungen. Wenn wir überhaupt noch bei der Clarity-Studie sind, Herr Nößler.
Nößler: Natürlich.
Scherer: Es geht ja immer darum, auch die Übertragbarkeit der Ergebnisse zu betrachten. Wie wurde die Patientenauswahl vorgenommen, die doch etwas selektiv ist. Dann haben wir die kurze Studiendauer. Innerhalb der kurzen Studiendauer vielleicht sechs Monate Progressionsverzögerung, die Sie mit ihrem Lineal gefunden haben. Dann natürlich auch damit einhergehend die unzureichende Untersuchung langfristiger Nebenwirkungen. Und ganz wichtig die nicht ausreichende Berücksichtigung von Variabilität in der Population.
Nößler: Das heißt, da machen Sie jetzt schon mal ein paar Fragezeichen dran, an die klinische Relevanz und Übertragbarkeit dieser Arbeit.
Scherer: Ja.
Nößler: Andere Frage: Wie oft oder regelmäßig lesen Sie eigentlich die Anhänge von solchen Veröffentlichungen, die Supplementary Appendices?
Scherer: Eigentlich nur, wenn berühmte Chefredakteure danach fragen.
Nößler: In diesem Fall wird es sich lohnen, würde ich mal sagen. Weil dort sind Subgruppenauswertungen drin, Herr Scherer, die in der Hauptpublikation gar nicht besprochen wurden.
Scherer: Lassen Sie mich raten: die fehlenden Effekte bei Jüngeren und bei den Frauen.
Nößler: So ist es. Nicht signifikant. Und bei den Frauen – Sie sagen es gerade – ist sogar das Mean fast null. Sie sind ja auch Studienautor und Sie machen Metaanalysen und Reviews. Ist das nicht eigentlich eine relevante Sache, die in der Hauptpublikation direkt zu adressieren wäre?
Scherer: Das ist in der Hauptpublikation zu adressieren und natürlich auch zu diskutieren. Das ist völlig klar. Warum das ins Supplement gepackt wurde, kann ich Ihnen nicht beantworten. Es gibt ja auch manchmal erratische Review-Verfahren, vielleicht wollten die Gutachter das, vielleicht waren es die Editoren, die dafür gesorgt haben, dass es ins Supplement kam. Ich kann es Ihnen nicht sagen.
Nößler: Da können wir nur Rätsel raten. Ergänzend, das wäre ein Lektüretipp, kann man sich anschauen, sind Forest-Plots, auch bei Asiaten und Europäern gibt es keine Signifikanz mehr in diesem einen Score CDR-SB. Das könnte aber, wenn ich es richtig sehe, eher daran liegen, dass es relativ kleine Populationen in der Studie waren. Ich würde gerne mal weitergehen mit dem Aspekt, nämlich: Wenn das jetzt zugelassen wird, müssen wir vielleicht erst mal gucken, für wen ist es überhaupt empfohlen. Herr Scherer, ich versuche es mal ganz kurz zusammenzufassen, was das CHMP aufgeschrieben hat. Das orientiert sich relativ an dem, was wir aus den USA von der FDA kennen. Und da bin ich mal gespannt, wie Sie das bewerten, was das für eine klinische Relevanz am Ende oder im klinischen Alltag für eine Relevanz haben wird. Es gibt ein Verordnungsausschluss, das Ganze soll nicht angewandt werden bei Menschen, die ApoE4-homozygot sind, weil es dort nichts bringt. Das hat die Clarity-AD-Studie gezeigt. Es soll außerdem nicht benutzt werden bei Menschen unter Antikoagulation. Weil wir haben diese ARIA-Problematik unter diesen Antikörpern. Da können Sie vielleicht gleich noch was zu sagen. Wenn ich jetzt aber schon mal höre: Antikoagulation ist ein Ausschluss – Herr Scherer, wir wissen doch, dass Vorhofflimmern ein Risikofaktor für Demenz ist.
Scherer: Ja. Und vor allem haben wir natürlich ganz viele Mischformen. Also die Patienten tun uns nicht den Gefallen, dass sie vornehmlich unter einheitlichen Alzheimer Demenzen leiden. Es gibt ein Großteil der Demenzen, bei denen es sich um Mischformen handelt, aus vaskulärer oder Alzheimer Demenz oder reine vaskuläre Demenzen. Und da haben wir natürlich auch bei diesen vaskulären Patienten die dabei, die antikoaguliert sind.
Nößler: Das heißt, da ist das Case-Finding dann das Problem eigentlich.
Scherer: Das ist ein relativ aufwendiges Case-Finding. Und das bei einer großen Zahl von Patienten – wir hatten es ganz am Anfang –, die sowieso altersbedingt subjektive Einschränkung in den kognitiven Funktionen haben.
Nößler: Herr Scherer, Antikörper ist ja nicht ganz ohne. Wir reden hier von ARIA. Das sollten Sie vielleicht noch mal aufklären.
Scherer: ARIA, das sind Amyloid-bedingte Bildveränderungen. Das sind die häufigsten Nebenwirkungen. Da gibt es Ödeme, da gibt es Mikroblutungen. Und die waren in dieser Phase-III-Studie auch gar nicht so selten. Das war bei 12 bis 17 Prozent der Patienten der Fall. Meistens ist es asymptomatisch. Aber die können auch schon mal gefährlich werden. Es gibt infusionsbedingte Reaktionen, grippeähnliche Symptome oder auch mal Reaktionen an der Infusionsstelle. Und zu den Langzeitrisiken, Herr Nößler, da wissen wir eben nichts.
Nößler: Weil wir 18 Monatsdaten haben. Gut. Langzeitgeschichten muss man dann noch weiter anschauen. Gucken wir uns das gerade noch mal an. Wer darf überhaupt da rein? Wie gehen wir da vor? Und da kommen wir wahrscheinlich gleich noch mal auf ARIA zurück. Das Ganze geht noch weiter. Die EMA, also dieses CHMP, wir sind ja noch in der Empfehlung. CHMP empfiehlt eine Beauflagung der Zulassung, dass die Leute in Register eingeschlossen werden sollen – so weit so vernünftig –, also Post-Marketing-Assessment. Und es gibt noch weitere Bedingungen. Es muss also eine MCI, Mild Cognitive Impairment vorliegen und eine leichte Demenz. Dann müssen Sie vorher Beta-Amyloid-Diagnostik machen. Das werden Sie wahrscheinlich, Herr Scherer, nicht mit einer PET-CT machen, sondern mit einer Liquor-Diagnostik, nehme ich mal an, weil PET-CT zahlt Ihnen keiner. Und dann müssen Sie noch eine genetische Testung auf ApoE4 machen und bei einer Homozygotie ist er raus. Jetzt geht das Ganze weiter: Das Ganze geben Sie dann alle zwei Wochen 10 mg pro Kilogramm über eine Stunde, das heißt, die müssen in irgendeine Ambulanz gehen, die Leute, und dann muss dieser ARIA-Check gemacht werden, Amyloid-related Imaging Abnormality, muss man davor machen. Dann bei der fünften, bei der siebten und bei der 14. Dosis. Das heißt, Sie schicken die Leute viermal in ein MRT rein. Jetzt bin ich mal gespannt, was Martin Scherer sagt, was da für eine Versorgungssituation auf uns zukommt.
Scherer: Sie haben es ein bisschen sehr kompliziert dargestellt. Also wenn man es so macht wie in er Studie, dann nimmt man MCI-Patienten, also Mild Cognitive Impairment oder eine leichte Alzheimer Demenz. Und braucht tatsächlich diese Amyloid-Ablagerungen, die man durch PET-CT oder durch Liquor-Analyse dann findet. Also dieser Vorlauf für eine Antikörperverschreibung, die nur im Frühstadium der Demenz wirksam ist, wo man die Langzeiteffekte nicht kennen und die teuer ist, müssen wir nicht lange drüber reden.
Nößler: Und Herr Scherer, Sie haben eben diese ARIA-Problematik angesprochen. Und da ist jetzt die Auflage – jedenfalls in der Zulassungsempfehlung von CHMP, so ist es bei der FDA auch in der Zulassung drin –, dass man eben die Leute ins MRT schicken muss, und zwar mindestens viermal, neben dem Aufwand für die Infusionen alle zwei Wochen über eine Stunde in der Ambulanz. Das ist jetzt nicht einfach nur eine Pille, die man da nimmt.
Scherer: Nein, das ist keine Pille, die man nimmt. Und die Bildgebung vor der Indikationsstellung und dann praktisch während des Monitorings – also der Aufwand ist einfach enorm, Herr Nößler. Es geht erst mal am Anfang darum, die Amyloid-Ablagerung zu sehen. Da brauchen wir entweder PET-CT oder eine Liquor-Diagnostik. Und dann ist es – wie Sie richtig auch angedeutet haben – um die Amyloid-bedingten Bildveränderungen, also die Nebenwirkungen – Ödeme, Mikroblutungen – zu identifizieren, braucht man im weiteren Verlauf dann noch MRTs. Also da fallen mir gleich ganz viele Dinge ein, warum das nicht geht. Das sind ältere Patienten, die haben noch andere Themen, die haben andere Erkrankungen. Dann müssen sie einen Termin kriegen. Dann haben sie vielleicht eine ewig lange Wartezeit auf MRT. Das hält die Bildgebungen auf, es macht einen Versorgungs-Overkill, eine Überdiagnostik, Überversorgungs-Overkill bei völlig ungesicherten Langzeiteffekten.
Nößler: Die Deutsche Gesellschaft für Neurologie hat mal vorgerechnet – es gibt ein Podcast von denen mit Prof. Jörg Schulz aus Aachen, der sitzt auch dem Netzwerk Gedächtnisambulanzen vor. Und er schätzt, das ist jetzt so eine Zahl, die er genannt hat, dass zwischen 5.000 und 10.000 Patienten in Deutschland in den nächsten eins, zwei, drei Jahren überhaupt dafür in Frage kommen. Wenn ich jetzt das nehme, was Sie alles gesagt haben, diese gesamte Diagnostikkette, diese ganze MRT, diese ganze Bildgebung, die Infusionsambulanzen mal 5.000 bis 10.000 – ich höre immer, dass wir einen Ärztemangel haben beziehungsweise die Praxen dicht sind. Und MRT-Termine kriegt man auch nicht so einfach, habe ich mal gehört. Das können wir uns sparen, oder?
Scherer: Ich hätte dann gerne einfach auch den Zeitaufwand mitgeschätzt, der dann auf die Praxen zukommt, die jetzt schon einen Aufnahmestopp haben, die jetzt schon lange Wartezeiten haben, die jetzt schon nicht genug Zeit haben, um die multimorbiden Patientinnen und Patienten zu behandeln und zu versorgen, die dringend auch Versorgungsbedarf haben.
Nößler: Und dann kommt dazu noch der Zeitaufwand in der hausärztlichen Praxis, um die Leute rauszufischen.
Scherer: Das ist genau das Entscheidende. Wenn 10.000 für die Therapie infrage kommen, dann muss man die erst mal finden – und das bedeutet einen riesigen Vorlauf – unter den 40 Prozent der älteren Bevölkerung diese 10.000 dann zu identifizieren. Ich habe da Déjà-vus, ich denke da mal wieder auch an das Gesundes-Herz-Gesetz. Das kriege ich wahrscheinlich auch nicht mehr so schnell wieder raus. Also das sind diese Ansätze, wo man innerhalb des nicht effizienten, nicht bedarfsgerecht funktionierenden Systems noch mal einen völlig neuen aufwendigen Versorgungs- und Diagnostikpfad implementiert, wo der Aufwand in überhaupt gar keinem Verhältnis zum Nutzen steht.
Nößler: Kann man sagen, Herr Scherer, das deutsche Gesundheitswesen bricht unter einem Antikörper zusammen?
Scherer: Es bricht jedenfalls unter ökonomisch getriebenen Einzellösungen zusammen, unter oftmals interessensgeleiteten Versorgungspfaden, die einfach einen unglaublichen Aufwand produzieren, bei völlig fraglichen Effekten.
Nößler: Vielleicht abschließend dazu noch eine Ergänzung. Was das dann hier kosten wird, das wissen wir sowieso noch nicht, weil es ist ja noch nicht zugelassen. Also gibt es auch keine Nutzenbewertung, also gibt es auch keine Preisverhandlung. Was wir aber wissen, Herr Scherer, dass der Hersteller letztes Jahr, als es in den USA zugelassen wurde, mitgeteilt hat, dass sie dort mit 26.500 US-Dollar pro Jahr Behandlungskosten für den Antikörper ins Rennen gegangen sind. Diese Preise sinken ja mit der Zeit auch, wenn die Versicherer dann die Rabatte verhandeln. Info dazu: das NICE hat die Erstattung zurückgewiesen, die werden das nicht erstatten in UK, im Übrigen auch bei Donanemab nicht, das ist ein anderer Antikörper, der noch kommt. Es gibt auch eine Arbeit – verlinken wir auch in den Shownotes –, die Martin Scherer schon erwähnt hat, von der European Alzheimer’s Disease Consortium, EADC. Die haben vorgerechnet, dass wenn man das wirklich für alle einsetzen würde, dann hätten wir in Europa Kosten von 133 Milliarden Euro pro Jahr nur für diesen Antikörper. Martin Scherer, wenn wir das jetzt mal alles zusammenbinden, was wir jetzt besprochen haben, wie Sie es einschätzen. Ich habe Sie ja nicht so richtig dazu bringen können, mal hier eine griffige Headline zuzulassen, da muss ich mich dann wieder drum kümmern. Wenn wir das jetzt noch mal alles irgendwie zusammen von dem, was wir wissen, von dem, was wir vermuten und von den Sorgen, was Sie geäußert haben: Was machen wir mit jetzt mit Lecanemab?
Scherer: Eine griffige Headline à la Nößler wäre: In die Tonne treten. Aber so einfach können wir es uns hier nicht machen, Herr Nößler. Der Podcast heißt EvidenzUpdate. Und am Ende des Tages müsse wir zu einer Risiko-Nutzen-Abwägung kommen. Vielleicht kann ich es für Sie noch mal auf den Punkt bringen. Der Nutzen ist, dass eine moderate Verlangsamung des Krankheitsverlaufs unter Verringerung der Amyloid-Last zu verzeichnen ist. Es können schwerwiegende Nebenwirkungen auftreten. Deshalb ist diese MRT-Überwachung nötig. Und die Patientenselektion ist extrem aufwendig. Das heißt mit anderen Worten: Es gibt keinen Grund, diesen Antikörper zu pushen, zu hypen und mit aller Gewalt in das System zu pressen. Unser System ist jetzt schon kurz vor dem Platzen. Und je mehr man da reindrückt und je mehr man da reinpresst, desto mehr Risse kriegt es. Es ist einfach hochgradig ineffizient. Und es werden unheimlich viele Ressourcen verpulvert an falscher Stelle, da, wo sie einen geringen Wirkungsgrad haben, sind nicht effizient. Und wenn man jetzt noch so einen gigantischen Aufwand für die Selektion von Patienten betreibt, die dann ein bisschen in einem bestimmten Stadium profitieren bei unklaren Langzeiteffekten, dann macht man das alles noch schlimmer. Aber verstehen Sie auch ein bisschen, Herr Nößler, meinen Unwillen, auf diese Leier immer wieder einzugehen? Weil das einfach auch sich wiederholende Prozesse sind. Ein extrem teures Element kommt aus der Entwicklung, kommt dann in die Zulassung, dann gibt es ein paar Studien dazu, die auch Effekte zeigen. Und dann haben wir die Selektionsthemen, wir haben die unklaren Langzeiteffekte. Wir haben meist Risiken, Kosten und den Aufwand im System. Das wiederholt sich immer wieder.
Nößler: Aber deswegen müssen wir es immer wiederholt besprechen.
Scherer: Da haben Sie natürlich recht, Herr Nößler. Wir müssen uns immer wieder damit befassen, aber es wiederholt sich eben auch immer wieder. Und manchmal wünscht man sich, man wäre in einem lernenden System, das die Fehler nicht immer wieder wiederholt. Aber so ist es mit der Geschichte auch. In der deutschen Geschichte, der Weltgeschichte wiederholen sich die Fehler immer wieder. Man lernt irgendwie nicht draus.
Nößler: Aber deswegen gibt es uns ja. Wir helfen wo wir können, damit wir vielleicht doch zu einem lernenden System werden. Und wenn ich Sie jetzt gerade eben in Ihrem zusammenfassenden, doch dann auch sehr detailreichen und wichtigen Ausführungen verstanden habe, da war für mich jetzt unausgesprochen auch eigentlich so ein Appell drin, nämlich: Bitte das jetzt nicht in die Versorgung pressen, auf der einen Seite, so wie vieles andere: Leistungsanreiz hier, Leistungsanreiz dort, Über-über-überversorgung.
Scherer: Richtig. Ja.
Nößler: Sondern den kleinen Nutzen, den wir hier sehen, bitte weiter erforschen, idealerweise noch mal in einer guten Studie mit einer ordentlichen Population, ohne dass jetzt hier irgendwas zusammenbricht, oder?
Scherer: Ja. Genau. Und als Wissenschaftler haben Sie mich damit absolut abgeholt. Und das ist auch in Ordnung, dass es da erste Schlussfolgerungen gibt, room for further research. Oder auch Fragestellungen zur Folgestudien. Aber allzu oft wird das übersprungen und der Shortcut ins System gewählt mit einer Riesenlobbyenergie, die sich da dann oft entfaltet. Ich kann es auch verstehen. Es sind Entwicklungskosten, die dahinterstehen. Und es müssen alle davon leben. Aber wie hat Herr Reinhardt so schön gesagt im Hartmannbund: Das Gesundheitssystem ist eben kein Selbstbedienungsladen.
Nößler: Das hat er gesagt. Und vielleicht abschließend noch ein ganz klein wenig Ehrenrettung für die Autoren der Publikation und natürlich des Sponsors Eisai and Biogen: Longer trials are warranted to determine the efficacy and safety of lecanemab. Das heißt, da sind sie beide sicher irgendwie einig. Herr Scherer, vielleicht noch der Versuch mal wieder: Wollen wir es mal wieder mit so einem Cliffhanger versuchen?
Scherer: Also wir gehen mit großen Schritten aufs Jahresende zu. Da freue ich mich sehr, wenn Sie überhaupt Zeit haben, kurz vor Silvester oder an Silvester.
Nößler: Mit Ihnen sitze ich doch gerne unterm Weihnachtsbaum.
Scherer: Wunderbar. Und dann machen wir einen schönen Jahresrückblick. Dann müssen wir uns auch noch mit der Niere befassen.
Nößler: Saure Nierchen zu Weihnachten.
Scherer: Ja wohl und einer neuen Leitlinie. Und das war es vom Cliffhanging. Nun überlasse ich Ihnen jetzt, uns ins Wochenende – oder wo schicken Sie uns hin? Es ist schwer zu sagen. Ich hätte gesagt: Schicken Sie uns in den Feierband, schicken Sie uns ins Wochenende. Aber man weiß ja nicht, wann unsere Podcasts gehört werden. Also schicken Sie uns in den Advent.
Nößler: In den Himmel, genau. In diesem Sinne, Herr Scherer, dann ist das quasi jetzt Ihr Adventsgruß gewesen mit diversen Ankündigungen. Wir werden die Versprechungen natürlich alle erfüllen. Wir grüßen alle da draußen, die uns zuhören, die treue Fans sind und sich immer auch kritisch an uns richtigen, vielleicht nicht immer sofort eine Antwort bekommen. Aber klar ist, wir gehen auf alles ein. Herr Scherer, ich freue mich auf das nächste Mal.
Scherer: Ich mich auch. Tschau, tschüss!